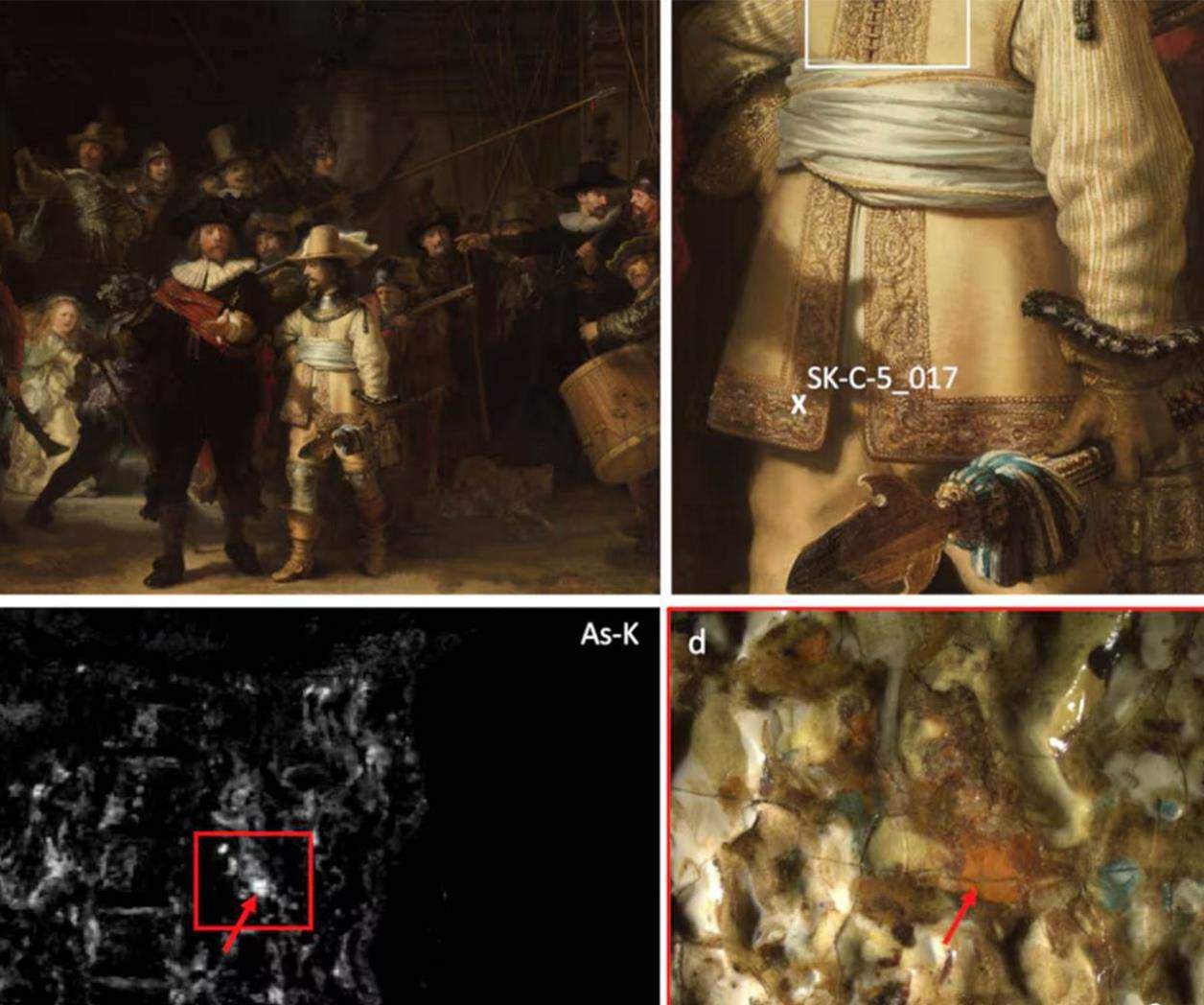
Rembrandt, el maestro neerlandés del Siglo de Oro, mezcló pigmentos de sulfuro de arsénico en su obra más famosa, La ronda de noche (1642). Una investigación del Rijksmuseum —que exhibe el cuadro— y la Universidad de Ámsterdam, que lo analizan desde 2019, sostiene que el artista creó así la ilusión de un hilo de oro en los bordados del jubón del teniente Willem van Ruytenburch. Es la figura vestida de amarillo en el centro del cuadro, y Rembrandt usó materiales llegados a través de rutas europeas de comercio.
"Pensábamos que Rembrandt había utilizado pigmentos naturales de sulfuro de arsénico, como el oropimente (amarillo) y rejalgar (rojo) para el efecto dorado de la almilla del teniente van Ruytenburch", explica, al teléfono, Fréderique Broers, una de las autoras principales del estudio, junto con Nouchka de Keyser. Sin embargo, la aplicación de técnicas de espectroscopia, microscopía y rayos X de alta tecnología a dos muestras obtenidas en 2019 ha revelado la presencia de otros dos componentes. Se hizo en el curso de la denominada Operación Ronda de Noche, y encontraron "pararrejalgar [formado como alteración del rejalgar], para el amarillo, y pararrejalgar semiamorfo, para el naranja/rojo. El segundo debió de obtenerse calentando o tostando el primero, logrando lo que llamamos sulfuro de arsénico artificial", dice.
Aunque los pigmentos arsenicales se aplicaban en la época a las frutas y flores de los bodegones, este hallazgo indica que Rembrandt innovó al usar algo más para los retratos. Su descubrimiento añade colores a la paleta del pintor y amplía la gama los materiales que se creía que podían obtener los artistas del siglo XVII en Ámsterdam.
La investigación ha sido publicada en la revista Heritage Science, y Broers admite que la terminología puede resultar algo confusa "porque se usan nombres distintos para cada uno de los pigmentos a lo largo del tiempo y en diferentes países". De todos modos, con ayuda de técnicas analíticas específicas, "que pueden distinguir dos moléculas incluso si ambas solo contienen arsénico y sulfuro, hemos podido diferenciarlos", asegura. Los pigmentos eran muy tóxicos en forma de polvo, aunque una vez mezclados con aceite de linaza para obtener la pintura se estabilizaban.
El pararrejalgar suele aparecer en las pinturas antiguas porque el rejalgar se degrada en este compuesto con el paso del tiempo, según la experta. Sin embargo, al estar distribuido junto con el pararrejalgar semiamorfo de forma homogénea y sin alteraciones en La ronda de noche, "creemos que el pintor los utilizó de forma deliberada para su efecto de reflejo dorado en el ropaje del teniente", señala Broers. Quería recrear una tela lujosa que acaparase la luz de la composición.
No está claro si Rembrandt compró ya lista la mezcla de rojo y amarillo ahora descubierta, o bien la hizo en su taller. Dado que Países Bajos no tiene recursos mineros significativos, "consideramos que llegaban a través de rutas comerciales en territorio alemán, Viena y Venecia, y el artista podía comprarlos en Ámsterdam", apunta el trabajo. Debido a ello, el uso de sulfuros de arsénico naturales y artificiales pudo ser más común de lo que se creía en el Siglo de Oro de la pintura neerlandesa. Sí disponía el artista de bermellón, "que es sulfuro de mercurio y también muy tóxico". "Y de colores tierra, logrados con hierro". El problema es que carecían de la profundidad de la mezcla con el rojizo y amarillento conseguida a base de sulfuro de arsénico.